Определение переваривающей способности пепсина желудочного сока
В четыре пробирки помещают следующие количества растворов в мл:

Желудочный сок добавляют после того, как во все пробирки раствор казеина и вода уже отмерены. Немедленно после добавления желудочного сока и встряхивания все пробирки одновременно ставят в водяную баню при 40°. Через 15 мин. пробирки ставят в ледяную воду и в каждую .пробирку добавляют по 2 мл 25 %-ного раствора уксуснокислого натрия. Содержимое пробирок перемешивают и измеряют степень мутности визуально или приборами: нефелометром или фотоэлектроколориметром. Степень мутности показывает количество непереварившегося белка и находится в обратной зависимости с активностью желудочного сока.
На мясокомбинатах при определении качества жиров, ферментных препаратов и пр. применяется фотоэлектроколориметр ФК-53.
Метод определения мутности растворов с фотоэлектроколориметром основан на уменьшении интенсивности света, прошедшего через мутную среду и измеренного фотоэлементом.
Фотоэлементы представляют собой приборы, преобразующие световую энергию в электрическую и заменяющие при измерениях глаз человека.
Если на пути пучка света, падающего на фотоэлемент, при соблюдении определенных условий попеременно ставить кюветы с растворами разной мутности, то на фотоэлемент будет попадать тем меньше света, чем мутнее раствор.
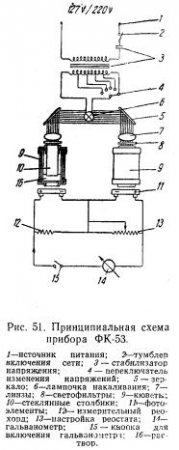
Принципиальная схема прибора ФК-53 (рис. 51) включает схему питания лампочки накаливания, оптическую схему и измерительную схему.
Схема питания лампочки накаливания. Источником света служит лампочка накаливания в 15 свечей, питающаяся от сети переменного тока через феррорезонансный стабилизатор напряжения 3. Включение в сеть производят тумблером 2. Переключатель напряжения 4 при определении активности желудочного сока устанавливают на 6 в.
Оптическая схема прибора состоит из двух зеркал 5, расположенных под углом 45° к оптической оси прибора, и двух линз 7. Свет лампочки 6, отразившись от поверхности зеркал, выходит из линз двумя параллельными пучками и, проходя через кюветы 9, нападает на фотоэлементы 11.
Один из параллельных пучков света проходит через кювету с дистиллированной водой, другой — через кювету с испытуемым мутным раствором. На каждый фотоэлемент падает световой поток различной силы, что учитывают посредством измерительной системы, основанной на компенсационном методе.
Измерительная схема представляет собой мостовую схему, в два плеча которой включены селеновые фотоэлементы, соединенные между собой одноименными полюсами, а в два других плеча — реостат настройки 13 и измерительный реохорд 12. В диагональ моста включен гальванометр 14, который играет роль нулевого прибора и реагирует на изменение фототока в цепи.
Различная освещенность фотоэлементов вызовет различную электродвижущую силу у каждого из них, что приведет к отклонению стрелки гальванометра от нулевого положения.
Компенсация схемы, а следовательно возвращение стрелки гальванометра к нулевому положению, осуществляется поворотом измерительного реохорда.
Перед измерением мутных растворе в производят настройку прибора. Для этого две кюветы наполняют дистиллированной водой, закрывают крышками с самыми длинными столбиками. Между стеклянной частью крышки и жидкостью не должно быть пузырьков воздуха. Поверхность кювет должна быть сухой. Кюветы ставят на чистый лист бумаги и убеждаются, что они не подтекают. Пользоваться подтекающей кюветой нельзя.
Вставляют кюветы в гнезда прибора и поворотом ручки реохорда совмещают нулевое деление шкалы реохорда с риской смотрового окна; включают вилку прибора в сеть переменного тока (127/220 в). Арретирный винт гальванометра ставит в положение «открыто»; ручку переключателя 1 (рис. 52) устанавливают в положение б; поворотом тумблера 3 включают прибор и дают ему прогреться в течение 5—10 мин. Нажатием кнопки включателя 6 подключают в цепь гальванометр и посредством реостата настройки 2 приводят стрелку гальванометра к нулю.

Далее заменяют правую кювету с водой на кювету с испытуемым раствором, закрывают той же самой крышкой и вставляют в гнездо прибора вместо снятой кюветы. Равновесие компенсационной схемы нарушается, и стрелка гальванометра отходит от нуля. Поворотом ручки реохорда при отрывистом нажатии кнопки стрелку гальванометра устанавливают на нуль и производят отсчет по шкале реохорда. Таким образом измеряют мутность растворов в каждой пробирке.
Устанавливают зависимость между количеством желудочного сока и степенью переваривания казеина, которая может быть выражена графически.
Приготовление раствора казеина. В химический стакан емкостью 100 мл помещают 0,25 г казеина по Гаммарстену, 25 мл дистиллированной воды и 6,25 мл 0,1N раствора едкого натра. Стаканчик помещают в водяную баню при температуре 50—70° и помешивают содержимое стеклянной палочкой до получения однородного слегка опалеоцирующего раствора. Содержимое стаканчика охлаждают до комнатной температуры и переносят при постоянном перемешивании в мерную колбу емкостью 250 мл, содержащую 100 мл 0,5%-ного раствора HCl. Стаканчик несколько раз тщательно ополаскивают 0,5%-ным раствором HCl, этой же кислотой доводят раствор до метки и тщательно взбалтывают.
Приготовление разбавленного желудочного сока. 10 мл желудочного сока помещают в мерную колбу емкостью 500 мл, добавляют 20 мл 10%-ного раствора соляной кислоты, доводят водой до метки и перемешивают.
Вместо желудочного сока можно применять порошок медицинского пепсина. Для этого 0,1 г препарата встряхивают с 50 мл дистиллированной воды в мерной колбочке емкостью 100 мл, добавляют при осторожном перемешивании 4 мл 10%-ного раствора соляной кислоты; полученный раствор доводят водой до метки, закрывают пробкой и взбалтывают до тех пор, пока не получится однородный раствор.
- Исследование желчи
- Открытие свободных аминокислот методом распределительной хроматографии на бумаге
- Реакция на свежесть мяса
- Обнаружение каротина в говяжьем жире хроматографическим методом
- Реакция на витамин А
- Обнаружение холестерина в мозге
- Исследование жиров
- Получение гиалуроновой кислоты
- Костная ткань
- Свойства желатина
- Получение желатина из сухожилий
- Минеральные вещества мышечной ткани
- Экстрактивные вещества мышечной ткани
- Ферменты мышечной ткани
- Разделение белков мышечной ткани
- Получение кристаллов гемина
- Спектроскопическое исследование гемоглобина и его производных
- Открытие минеральных веществ в крови
- Разделение белков плазмы и сыворотки
- Реакции на наличие ферментов
- Влияние осмотического давления на эритроциты
- Приготовление стабилизированной и дефибринированной крови
- Реакция на конечные продукты обмена белков
- Брожение
- Гликолиз
- Реакция на наличие ферментов
- Активаторы ферментов
- Зависимость действия ферментов от pH
- Специфичность ферментов
- Неустойчивость ферментов к действию высокой температуры