Химическая обработка сырья для получения желатина
Удаление минеральной части достигается мацерацией (от латинского maceratio — размягчение), заключающейся в обработке кости раствором соляной кислоты (можно применять растворы других кислот, образующих с кальцием растворимые соли и не оказывающих значительного химического воздействия на коллаген):
Ca8 (PO4)2 + 6HCl = 3CaCl2 + 2H3PO4.
В результате мацерации получается оссеин.
Для получения желатина оссеин или другое сырье, содержащее коллаген, необходимо подвергнуть специальной химической обработке — золке, которую обычно производят насыщенным раствором Ca(OH)2.
В результате золки происходит набухание коллагена, удаляются балластные белки (альбумины, глобулины, муцины, мукоиды), входящие в состав основного вещества соединительной ткани, омыляются жиры и в тех случаях, если используются обрезки шкур, ослабляется связь дермы с волосом и эпидермисом. Балластные белки необходимо удалять потому, что они являются одной из причин получения мутного желатина.
Омыление жиров в процессе золки сырья также необходимо, так как наличие их в желатине снижает его качество, придавая ему мутность и влияя на крепость студня.
Чрезвычайно важный момент в подготовке коллагена к выварке — набухание. Набухший коллаген превращается в желатин быстрее при более низкой температуре (55—60°), чем коллаген, не подвергшийся такой обработке. Невываренный остаток невелик. Это позволяет получить желатин высокого качества. Коллаген незоленых сухожилий превращается в желатин медленно; температура варки высокая (85—90°); остается большой невываренный остаток; при этом получается технический желатин.
Качество желатина зависит от содержания в нем полипептидов. Повышение температуры и продолжительности обработки коллагена водой способствует большему гидролизу, а следовательно, снижению вязкости и желирующей способности желатина, т. е. снижению его качества. Продукт, содержащий большое количество полипептидов, представляет собой клей. Чем больше в желатине полипептидов, тем ниже его желирующая способность и крепость студня, но выше способность к склеиванию. Следовательно, образование большого количества полипептидов при производстве желатина приводит к получению клея. Этот продукт дешевле желатина. Получают его более рентабельными способами и из более широкого ассортимента сырья. Очень глубокий гидролиз желатина может привести в конечном итоге к потере не только желирующей, но и клеящей способности.
Сильное набухание коллагена может быть достигнуто в результате обработки коллагенсодержащего сырья растворами щелочей, кислот, некоторых солей.
Если общая обводненность на 100 г сухой дермы при pH 5— 7 составляет примерно 200 г, то при pH 2—3 или pH 11—13 она резко повышается. Изменение степени набухания дермы в зависимости от величины pH представлено на рис. 13.
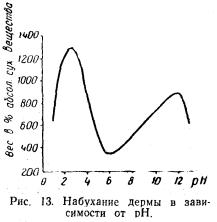
При набухании коллагена в кислых и щелочных растворах происходит необратимое частичное ослабление межмолекулярных связей; пучки коллагена разрыхляются, а также разрушаются мембраны, ограничивающие пучки коллагеновых волокон. Благодаря этому в процессе варки облегчается переход коллагена в желатин.
С повышением продолжительности золки увеличивается разрыхление коллагеновых пучков; этот процесс необратим. Влияние длительности золки на разрыхление пучков дермы и выход желатина приведены в табл. 13.

Продолжительная золка, особенно при повышенной температуре, приводит к потерям коллагена вследствие гидролиза. На производстве наиболее распространенным способом золки является обработка сырья насыщенным раствором гидрата окиси кальция (известковым молоком). Ценность этого способа с химической точки зрения заключается в том, что гидролиз коллагена в этом случае незначителен.
Растворы едкого натра резко ускоряют процесс золки, но способствуют значительному распаду коллагена. Это обстоятельство препятствует практическому применению едкого натра.
При золке гидроокисью кальция последняя содержится в сырье частично в виде капиллярно поглощенного раствора, частично химически связанной с белками. Слабая диссоциация соединения гидроокиси кальция с коллагеном не позволяет разрушить его промывкой водой. Поэтому для удаления ионов кальция из набухшего сырья прибегают к процессу ионного обмена посредством кислот или кислых солей. Обычно пользуются соляной кислотой, так как она образует с кальцием хорошо растворимую соль CaCl2:
Ca(ОH)2 + 2HCl = CaCl2 + 2H2О.
Этот процесс называется нейтрализацией. После нейтрализации и промывки сырья приступают к выварке желатина.
- Костная ткань
- Хрящевая ткань
- Химический состав сырья для получения желатина
- Химический состав соединительной ткани
- Химия соединительной ткани
- Химизм мышечной работы
- Ферменты мышечной ткани
- Липоиды и жиры мышечной ткани
- Минеральные вещества мышечной ткани
- Экстрактивные вещества мышечной ткани
- Белки мышечной ткани
- Химия мышечной ткани
- Денатурация белков крови
- Использование крови для технических целей
- Использование крови для лечебных целей
- Использование крови для пищевых целей
- Порча крови
- Химический состав плазмы крови
- Гемолиз крови
- Химия эритроцитов
- Химический состав крови
- Постоянство состава и физико-химические свойства крови
- Дефибринирование крови
- Стабилизация крови
- Свертывание крови
- Химия крови
- Автолиз
- Гниение белков в кишечнике
- Обмен сложных белков
- Образование специфических веществ