Классификация ферментов
Некоторые ферменты, например трипсин и пепсин, сохранили название, данное им при их открытии. Однако в соответствии со сказанным трипсин может быть назван триптазой, а пепсин — пепсиназой.
Классификация ферментов основана на характере производимого ими действия.
1. Гидролазы:
- протеазы (пепсин, трипсин и др.);
- эстеразы (липазы, фоефатазы и др.);
- карбогидразы (лактаза, амилаза и др.);
- амидазы (уреаза, гистозим и др.).
2. Фосфорилазы.
3. Окислительно-восстановительные ферменты:
- оксидазы (тирозиназа и др.);
- дегидразы (лактикодегидраза и др.);
- пероксидазы (липоксидаза и др.);
- каталазы.
4. Десмолазы (карбоксилаза, альдолаза и др.).
5. Феразы (фосфоферазы, аминоферазы и др.).
Гидролазы
К гидролазам относятся ферменты, катализирующие реакции расщепления и синтеза веществ, происходящих с участием воды. При помощи их сложные органические вещества расщепляются на более простые, и, наоборот, из простых веществ синтезируются сложные. Поскольку расщепление с присоединением молекулы воды называется гидролизом, то ферменты, катализирующие подобные реакции, называются гидролазами.
Протеазы. К протеазам принадлежат ферменты, катализирующие реакции расщепления пептидных связей в белках и промежуточных продуктах распада и синтеза белков. Расщепление дипептида глицил-глицина под действием дипептидазы протекает следующим образом:
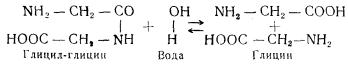
Представителями протеаз являются пепсин, трипсин, катепсин, аминопептидаза и др.
Амидазы. К амидазам относятся ферменты, ускоряющие реакции расщепления связи между углеродом и азотом в таких соединениях, как мочевина и амиды аминокислот.
Уреаза расщепляет мочевину в присутствий воды на аммиак и углекислый газ:
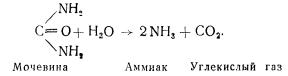
Эстеразы. К эстеразам относятся ферменты, ускоряющие реакции распада и синтеза веществ, построенных по типу сложных эфиров. Представителями эстераз являются липазы, действующие на жиры, фосфатазы — на фосфатиды и на многие эфиры фосфорной кислоты.
Химизм процесса, катализируемого липазами, можно представить следующим образом:
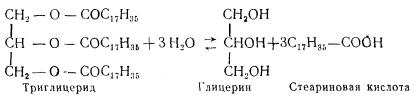
В результате этой реакции жир распадается на глицерин и жирные кислоты.
Карбогидразы. Ферменты, катализирующие реакции гидролиза и синтеза углеводов, называются карбогидразами. Схематически реакции, ускоряемые карбогидразами, можно представить в следующем виде:
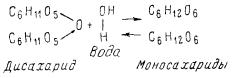
Представителями карбогидраз являются мальтаза, лактаза, сахараза, амилаза, целлюлаза и др.
Расщепление сложной молекулы полисахарида происходит с участием двух ферментов. Гликоген расщепляется до глюкозы амилазой и мальтазой; под влиянием амилазы — до мальтозы, а под действием мальтазы — до глюкозы.
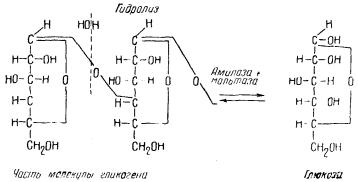
В результате полного гидролиза гликогена образуется большое число (n) молекул глюкозы.
Фосфорилазы
Фосфорилазы принадлежат к ферментам, ускоряющим процесс фосфоролиза, т. е. реакции расщепления и синтеза некоторых сложных органических соединений (крахмала, гликогена) с участием фосфорной кислоты. Название «фосфоролиз» указывает на сходство этого процесса с гидролизом. При фосфоролизе в реакции расщепления роль воды выполняет фосфорная кислота. В качестве примера приводится реакция расщепления гликогена под действием фосфорилазы:
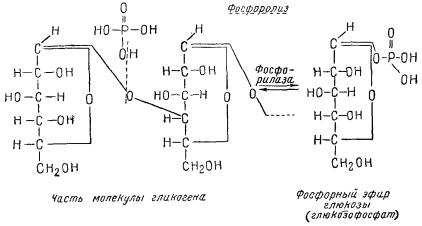
Таким образом, в результате фосфоролиза гликоген расщепляется с образованием большого числа молекул фоcфорилированной глюкозы.
При сравнении процессов гидролиза и фосфоролиза видно, что в первом случае расщепление происходит с присоединением элементов частицы воды, а во втором — фосфорной кислоты.
Окислительно-восстановительные ферменты
Окислительно-восстановительные ферменты катализируют реакции, связанные с переносом электронов и атомов водорода.
Оксидазы катализируют реакции окисления определенных органических соединений путем переноса электронов и атомов водорода непосредственно на молекулярный кислород воздуха. Схематически окисление вещества (субстрата) можно представить следующей реакцией:
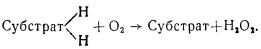
Дегидразы ускоряют реакции отнятия водорода от определенных органических веществ и передают его на промежуточные соединения. В качестве примера можно привести реакцию образования молочной кислоты из пировиноградной, катализируемой ферментом лактикодегидразой:
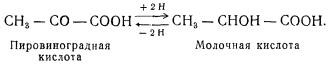
Пероксидазы катализируют реакции окисления некоторых органических веществ за счет кислорода перекисей (перекиси водорода, органических перекисей). Реакции с участием пероксидаз можно представить в виде следующей схемы:
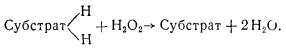
Каталазы являются спутниками окислительно-восстановительных ферментов. Они катализируют только реакцию распада перекиси водорода на молекулярный кислород и воду и этим освобождают клетки от губительного действия перекиси водорода, образующейся при многих окислительно-восстановительных процессах, протекающих в организме:
2H2O2 → 2H2O + O2.
Десмолазы
Десмолазы катализируют реакции расщепления связи между атомами углерода. В качестве примера приводится реакция отщепления углекислого газа от пировиноградной кислоты под действием карбоксилазы:
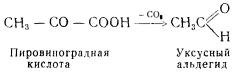
Эта реакция катализируется ферментом карбоксилазой, простетической группой которой является фосфорилированный витамин В1.
Феразы
Феразы катализируют реакции переноса некоторых атомных группировок с одного соединения на другое. При помощи фосфофераз осуществляется перенос остатка фосфорной кислоты, аминофераз — аминогруппы, метилфераз — метальной группы. Суммарный эффект действия аминофераз можно представить следующей реакцией:
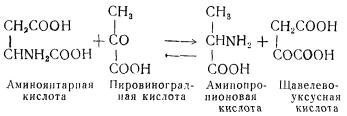
Активной группой аминофераз является фосфорилированное производное витамина B6.
- Свойства ферментов
- Химическая природа ферментов
- Ферменты
- Минеральные соли
- Полисахариды
- Дисахариды
- Моносахариды
- Углеводы
- Липиды
- Классификация белков
- Биологические особенности белков
- Изоэлектрическая точка белков
- Коллоидальная природа белков
- Молекулярный вес белков
- Денатурация белков
- Методы выделения белков
- Теории строения белков
- Способ связи аминокислот в белковой молекуле
- Аминокислоты
- Белки
- Химия важнейших веществ, входящих в состав организма животных
- Активная реакция среды
- Значение воды для жизни организма
- Элементарный состав организмов
- Понятие об обмене веществ
- Производство зубных щеток
- Производство гребней и расчесок
- Производство костяных (бельевых) пуговиц
- Сырье для производства предметов широкого потребления
- Производство желудочного сока