Изоэлектрическая точка белков
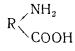
Вследствие наличия свободных карбоксильных и аминных групп белки, подобно аминокислотам, также являются амфотерными электролитами, т. е. диссоциируют как кислоты и как основания.
В водном растворе значительная часть молекул белка находится в ионизированном состоянии. Схематически процесс диссоциации белковых молекул в воде можно изобразить следующим образом:
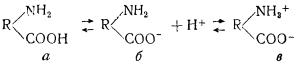
Как видно из уравнения, свободная карбоксильная группа белковой молекулы а диссоциирует на ион водорода и отрицательно заряженный остаток белка — анион б. В способности образовывать ионы водорода проявляются кислотные свойства белков. Основные свойства белков проявляются в их способности присоединять ионы водорода к аминогруппам. В результате такого превращения образуются частицы белка в, несущие одновременно положительный и отрицательный заряды.
В зависимости от реакции раствора белок может вести себя как кислота и как основание. В кислом растворе он ведет себя как основание, так как в этом случае благодаря наличию в растворе значительного количества ионов водорода кислотная диссоциация белка подавляется. В щелочном растворе он диссоциирует как кислота, так как в этом случае подавляется диссоциация основных групп белка. Например, белки крови реагируют как слабые кислоты, так как реакция крови слабо щелочная.
При пропускании через раствор белка электрического тока молекулы перемещаются в зависимости от реакции среды к положительному или отрицательному полюсу. Ho при определенной концентрации ионов водорода в растворе, т. е. при определенном pH, количество положительных и отрицательных зарядов в молекуле белка может оказаться одинаковым. В этом случае молекулы белка будут электронейтральны, т. е. при пропускании через такой раствор электрического тока они не будут передвигаться ни к аноду, ни к катоду.
Равенство положительных и отрицательных зарядов в молекуле белка, равенство кислой и основной степеней диссоциации называется изоэлектрическим состоянием. Величина pH среды, при которой белки находятся в изоэлектрическом состоянии, называется изо электрической точкой.
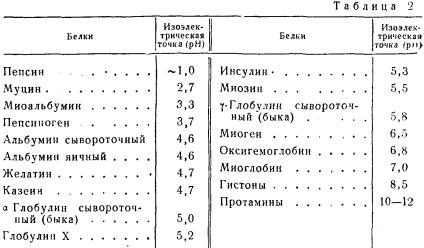
У большинства белков преобладают кислотные свойства, и их газоэлектрическая точка находится в кислой среде (альбумины, глобулины, казеин и пр.). У белков, содержащих очень много диаминокислот, наиболее сильно выражены основные свойства; изоэлектрическая точка этих белков находится в щелочной среде (протамины, гистоны).
Значения изоэлектрической точки некоторых белков приведены в табл. 2.
В изоэлектрической точке белки легко выпадают в осадок, в наименьшей степени набухают и имеют наименьшую вязкость.
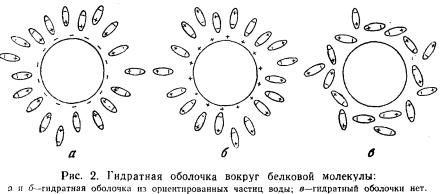
Легкость осаждения объясняется тем, что в изоэлектрической точке белковые частицы не имеют заряда. Наличие заряда — один из важнейших факторов устойчивости белкового раствора; другой важнейший фактор — наличие гидратной оболочки из ориентированных частиц воды вокруг белковой молекулы (рис. 2, а, б). Например, при pH 3,5 молекула альбумина реагирует как основание и несет положительный заряд; при pH 6,6 молекула альбумина реагирует как кислота и имеет отрицательный заряд.
Вода является диполем, поэтому ее частицы располагаются вокруг белковой молекулы в зависимости от заряда последней. Например, молекула сывороточного альбумина в изоэлектрической точке при pH 4,6 является электронейтральной; в этом случае вокруг белковой молекулы не образуется ориентированной гидратной оболочки (рис. 2, в).
Из сильно подкисленного или щелочного раствора белок вследствие наличия электрического заряда не выпадает в осадок даже при кипячении.
При осаждении белков необходимо стремиться к тому, чтобы разрушить защитную водную оболочку и снять электрический заряд. Поэтому осаждать белки солями лучше в изоэлектрической точке. Полное осаждение белка может быть достигнуто путем разрушения водной оболочки и снятия электрического заряда.
Степень осаждения белков солями тяжелых металлов, которыми часто пользуются при анализе белков, зависит от природы осаждающего иона. Если осаждающий ион имеет положительный заряд, то реакцию следует проводить в щелочной среде; если отрицательный, то в кислой среде, с тем чтобы соответственна подавить диссоциацию основной или кислотной групп белка.
- Коллоидальная природа белков
- Молекулярный вес белков
- Денатурация белков
- Методы выделения белков
- Теории строения белков
- Способ связи аминокислот в белковой молекуле
- Аминокислоты
- Белки
- Химия важнейших веществ, входящих в состав организма животных
- Активная реакция среды
- Значение воды для жизни организма
- Элементарный состав организмов
- Понятие об обмене веществ
- Производство зубных щеток
- Производство гребней и расчесок
- Производство костяных (бельевых) пуговиц
- Сырье для производства предметов широкого потребления
- Производство желудочного сока
- Производство инсулина-сырца
- Производство жидких препаратов
- Производство сухих препаратов
- Основные процессы в производстве органопрепаратов
- Сбор и обработка эндокринного, ферментного, специального сырья
- Производство органопрепаратов
- Производство сухого яичного порошка
- Производство меланжа
- Покрытие яиц искусственными оболочками
- Известкование яиц
- Брак яиц
- Структура, химический состав и биологические свойства яйца