Активная реакция среды
Под активной реакцией среды понимают концентрацию в растворе ионов водорода или ионов гидроксила.
Многие вещества (электролиты) в водном растворе распадаются на ионы. В зависимости от природы электролита степень распада (диссоциации) различна. Чистая вода является очень слабым электролитом, диссоциирующим на ионы водорода и гидроксила:
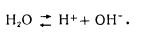
Количество ионов водорода и гидроксила в чистой воде ничтожно и составляет 0,0000001 г.
Кислоты в водных растворах диссоциируют на ион водорода и соответствующий анион:
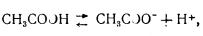
а основания — на ион гидроксила и соответствующий катион:
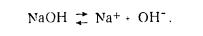
Если в растворе концентрация ионов водорода равна концентрации ионов гидроксила ([Н+]=[ОН-]), реакция нейтральная; если концентрация ионов водорода меньше, чем концентрация ионов гидроксила ([H-](ОН ]), реакция кислая.
При одинаковой нормальности растворов уксусной и соляной кислот активная реакция в растворе уксусной кислоты меньше, чем в растворе соляной кислоты, так как уксусная кислота диссоциирует слабее, чем соляная, вследствие чего ионов водорода в растворе уксусной кислоты меньше, чем в растворе соляной кислоты.
Таким образом, нейтральная реакция среды характеризуется равенством концентраций ионов Н+ и OH- в растворе, кислая — преобладанием ионов водорода над ионами гидроксила, щелочная — преобладанием ионов гидроксила над ионами водорода. С увеличением концентрации ионов водорода в растворе уменьшается концентрация ионов гидроксила, и наоборот. Даже в очень кислых растворах всегда имеется ничтожное количество ионов гидроксила и в очень щелочных — ионов водорода. Поэтому активную реакцию среды можно охарактеризовать содержанием ионов водорода или содержанием ионов гидроксила. Принято активную реакцию среды выражать через концентрацию ионов водорода, которая для воды равна 1*10в-7. Чтобы не оперировать в практической работе с такими неудобными числовыми значениями, активную реакцию среды большей частью выражают через водородный показатель pH.
Водородный показатель — это логарифм концентрации ионов водорода, взятый с обратным знаком:
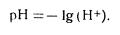
Изменения pH в области от 0 до 7 характеризуют кислую, при pH 7 нейтральную и pH от 7 до 14 щелочную реакцию.
Различные химические процессы протекают неодинаково, в зависимости от того, будет ли реакция среды кислой, нейтральной или щелочной. Так же обстоит дело и с процессами, протекающими в клетках живого организма, и здесь реакция среды играет большую роль. Это подтверждается тем, что постоянство реакции крови и тканевых жидкостей, например лимфы, поддерживается с большой точностью, несмотря на то, что вещества, образующиеся в тканях в процессе обмена, стремятся ее нарушить.
Свойства белков проявляются в строгой зависимости от характера реакции среды. Особенно важно значение активной реакции среды для ферментативных процессов.
Реакция среды крови и других тканей и органов слабощелочная, близкая к нейтральной. В крови постоянство pH поддерживается в очень узких пределах (7,3—7,4). Сдвиг pH в кислую или щелочную сторону является результатом каких-либо нарушений, происходящих в организме.
Постоянство pH крови поддерживается путем химической регуляции буферными системами, имеющимися в крови, и удалением конечных продуктов обмена легкими и почками. Легкие удаляют кислые продукты — углекислоту, почки — фосфаты и аммиак, последний в основном после превращения в мочевину.
Под буферным действием понимают способность раствора сопротивляться изменениям pH, которые должны были бы произойти вследствие добавления кислоты или щелочи.
Буферные системы крови и тканевых жидкостей могут поддерживать постоянный pH при образовании кислот и оснований, освобождающихся в процессе обмена.
Из буферных систем наибольшее значение в организме имеют белки, а также минеральные соединения — бикарбонаты и фосфаты натрия и калия. Буферными системами крови являются: кароонатная — H2CO3/NaHCO3, фосфатная NaH2PO4/NaHPO4 и белковая белок-кислота/белок-соль.
В организме при взаимодействии бикарбоната натрия NaHCO3 с выделившейся в процессе обмена фосфорной кислотой образуется угольная кислота:
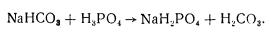
Угольная кислота, являясь очень нестойкой, быстро распадается и выводится из организма вместе с выдыхаемым воздухом в виде воды и углекислого газа. Таким образом обеспечивается постоянство pH крови. Так же противодействуют изменениям pH соли фосфорной кислоты. Например, при взаимодействии молочной кислоты с двузамещенным фосфорнокислым натрием образуется натриевая соль молочной кислоты и однозамещенный фосфорнокислый натрий:
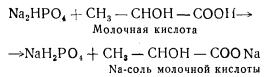
Аммиак, образующийся в процессе обмена оснований, связывается со свободной угольной кислотой, в результате чего образуется бикарбонат аммония:
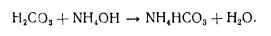
Важнейшим буферным веществом цельной крови является белок гемоглобин, который благодаря кислотным свойствам может связывать основания и образовывать соли, например Na-гемоглобин.
Буферную способность крови можно показать на следующем примере: чтобы сдвинуть pH сыворотки крови в щелочную сторону до pH 8,2, нужно добавить щелочи в 70 раз больше, чем к воде, а чтобы сдвинуть pH крови до 4,4, нужно добавить к крови в 327 раз больше соляной кислоты, чем к воде.
- Значение воды для жизни организма
- Элементарный состав организмов
- Понятие об обмене веществ
- Производство зубных щеток
- Производство гребней и расчесок
- Производство костяных (бельевых) пуговиц
- Сырье для производства предметов широкого потребления
- Производство желудочного сока
- Производство инсулина-сырца
- Производство жидких препаратов
- Производство сухих препаратов
- Основные процессы в производстве органопрепаратов
- Сбор и обработка эндокринного, ферментного, специального сырья
- Производство органопрепаратов
- Производство сухого яичного порошка
- Производство меланжа
- Покрытие яиц искусственными оболочками
- Известкование яиц
- Брак яиц
- Структура, химический состав и биологические свойства яйца
- Прием и сортировка яиц
- Заготовка и транспортировка яиц
- Расчеты при переработке крови убойных животных
- Требования, предъявляемые к готовой продукции альбумина
- Производство кровяной муки
- Производство гематогена
- Производство светлого и темного пищевого альбумина
- Производство черного и светлого технического альбумина
- Сушка крови
- Консервирование крови