Способ связи аминокислот в белковой молекуле
Более ста лет известна биуретовая реакция, заключающаяся в образовании характерной окраски при добавлении к щелочному раствору белка нескольких капель разбавленного раствора медного купороса. Такую же реакцию дают биурет (NH2—CO—NH—CO—NH2) и ряд других соединений, для которых общим является наличие группы —CO—NH—, повторяющейся не менее двух раз.
Еще в 1888 г. основоположник русской биохимии А. Я. Данилевский высказал предположение, что характерным типом связи аминокислот в белковой молекуле является связь —CO—NH—. Позже эта связь была названа пептидной; ее образование можно представить следующим образом:
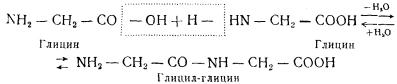
Карбоксильная группа одной аминокислоты реагирует с аминной группой другой с выделением молекулы воды. Пo освободившимся валентностям углерод и азот двух остатков аминокислот соединяются с образованием пептидной связи.
Полученное соединение называется дипептидом. При присоединении к этому дипептиду еще одной аминокислоты, например аланина, получается трипептид, который может быть назван глицил-глицил-аланин. Таким же путем могут быть получены соединения с большим числом остатков аминокислот. Полное название сохраняет остаток той аминокислоты, в которой сохранилась карбоксильная группа, в остальных меняется окончание «н» на «л» Эти соединения называются полипептидами и могут быть получены синтетически и путем гидролиза в качестве промежуточных продуктов распада белка,
Продукты, образующиеся при гидролизе белков, могут очень сильно различаться по молекулярному весу.
Гидролиз белка происходит с образованием следующих продуктов распада:
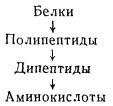
Пептидная связь является главенствующим типом связи в белковой молекуле; она может существовать в нескольких формах.
Белки обладают большой способностью к различным реакциям, что обусловливается наличием активных групп: аминогруппы — NH2, карбоксильной — СООН, гидроксильной — ОН, пептидной связи — CO — NH —, сульфгидрильной группы — SH и т. д.
Исключительное разнообразие в белковой молекуле активных групп и связей, способных непрерывно реагировать между собой и с другими веществами, позволяет белкам живого организма постоянно находиться в динамическом состоянии. Энгельс писал: «Жизнь есть способ существования белковых тел, и этот способ существования состоит по своему существу в постоянном самообновлении химических составных частей этих тел».
- Аминокислоты
- Белки
- Химия важнейших веществ, входящих в состав организма животных
- Активная реакция среды
- Значение воды для жизни организма
- Элементарный состав организмов
- Понятие об обмене веществ
- Производство зубных щеток
- Производство гребней и расчесок
- Производство костяных (бельевых) пуговиц
- Сырье для производства предметов широкого потребления
- Производство желудочного сока
- Производство инсулина-сырца
- Производство жидких препаратов
- Производство сухих препаратов
- Основные процессы в производстве органопрепаратов
- Сбор и обработка эндокринного, ферментного, специального сырья
- Производство органопрепаратов
- Производство сухого яичного порошка
- Производство меланжа
- Покрытие яиц искусственными оболочками
- Известкование яиц
- Брак яиц
- Структура, химический состав и биологические свойства яйца
- Прием и сортировка яиц
- Заготовка и транспортировка яиц
- Расчеты при переработке крови убойных животных
- Требования, предъявляемые к готовой продукции альбумина
- Производство кровяной муки
- Производство гематогена