Определение общего количества азота по Кьельдалю
Впервые метод Кьельдаля был применен для определения азота в мясе и различных тканях без предварительного их высушивания и обезжиривания великим русским физиологом И. П. Павловым совместно с Д. П. Павловым.
Сущность метода определения общего количества азота сводится к мокрому озолению органических веществ исследуемой ткани серной кислотой при нагревании в присутствии катализаторов. В процессе озоления органические вещества исследуемой ткани сгорают: углерод до CO2, водород до H2O, сера до SO2, азот превращается в NH3, ив которого при реакции с серной кислотой образуется (NH4)2SO4. Часть серной кислоты, окисляющей органические вещества, восстанавливается до SO2. Аммиак из сернокислого аммония вытесняется щелочью по реакции
(NH4)2 SO4 + 2NaOH— → Na2SO4 + 2NH3 + 2Н2О.
и отгоняется в титрованную кислоту. По количеству связавшейся с аммиаком кислоты судят о количестве азота.
Ход определения. Навеску ткани около 1 г берут по разности непосредственно в колбу Кьельдаля емкостью 100 мл. Навеска по разности берется следующим образом: в стеклянный стаканчик с притертой крышкой и стеклянной палочкой помещают исследуемый объект, например мясной фарш. Взвешивают, записывают вес, отделяют небольшой кусочек фарша палочкой и помещают его в колбу Кьельдаля; стаканчик с фаршем вновь взвешивают. По разности весов определяют вес фарша, взятого для анализа.
Навеску исследуемой ткани или точно отмеренное количество исследуемой жидкости заливают 5—10 мл концентрированной серной кислоты. Для ускорения озоления в колбу добавляют около 0,2 г сернокислой меди и 1,5 г сернокислого калия. Далее смесь нагревают, причем колбу ставят наклонно на плитку, чтобы при кипячении не происходило выбрасывания содержимого.
Вначале нагревание ведут осторожно. Озоление смеси продолжают до полного исчезновения бурой, а затем желтой окраски. Следы желтой окраски характеризуют неполноту сгорания. При полном сгорании раствор становится бесцветным или зеленоватым. Если на горлышке колбы остались обуглившиеся частицы, колбе дают остыть и затем смывают их водой внутрь колбы, после чего продолжают озоление.
После озоления и охлаждения содержимое колбы смывают дистиллированной водой через воронку в мерную колбу на 200 мл и доводят до метки.
Для отгонки аммиака применяют прибор, изображенный на рис. 44. В приемную колбу 5 отмеряют 10 мл 0,05 N серной кислоты, добавляют три-пять капель индикатора (метилрот) и устанавливают ее под холодильник, погрузив конец холодильной трубки в кислоту. Это необходимо потому, что первые порции аммиака летят в виде газа. Нагревают воду в парообразователе 1 до кипения.
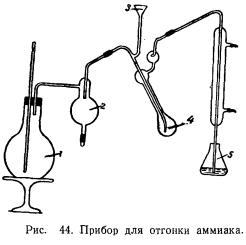
В отгонную колбу 4 при помощи -воронки 3 вводят 5 мл испытуемого раствора, затем 2—3 мл дистиллированной воды, 10—12 мл 33%-ной щелочи и еще раз 2—3 мл воды. Количество щелочи должно быть взято в избытке по сравнению с кислотой. Его можно рассчитать, исходя из количества кислоты, взятой для сжигания, с учетом последующего разведения. Воронку 3 снимают; отверстие закрывают стеклянной палочкой. Реакция жидкости должна быть щелочной. Это легко определить по появлению синей окраски, обусловленной гидратом окиси меди.
Пускают пар в колбу 4, закрывая отверстие сосуда 2 стеклянной палочкой. Через 15 мин. после отгонки конец холодильной трубки вынимают из кислоты.
Отгонка продолжается 20—25 мин. Пo прошествии этого времени прекращают впуск пара в отгонную колбу, открывая отверстие сосуда 2, Конец холодильной трубки обмывают дистиллированной водой, проверяют полноту отгонки по красной лакмусовой бумажке, снимают приемную колбу 5 и производят титрование 0,05 N раствором щелочи.
Предварительно 10 мл 0,05 N раствора кислоты оттитровывают 0,05 N раствором щелочи с индикатором метилрот.
Содержание азота выражают в процентах; расчет производят по следующей формуле:
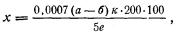
где: а — количество 0,05 N раствора щелочи, пошедшее на титрование 10 мл 0,05 N раствора кислоты, в мл;
б — количество 0,05 N раствора щелочи, пошедшее на титрование испытуемого раствора, в мл;
е — навеска в г;
к — поправка к раствору щелочи;
200 — разведение;
5 — количество испытуемого раствора, взятое для отгонки из колбы емкостью 200 мл;
0,0007 — количество азота, эквивалентное 1 мл 0,05 N раствора щелочи, в г.
- Активная реакция среды
- Определение содержания золы в тканях
- Определение содержания влаги в тканях
- Защитные покрытия
- Упаковки для хранения продуктов
- Влияние радиоактивных излучений на сохранность мясопродуктов
- Влияние углекислого газа на сохранность мяса и других продуктов
- Влияние ультрафиолетовых лучей на мясо и мясопродукты
- Фитонциды
- Антибиотики
- Консервирующие химические средства
- Повышение устойчивости мяса при хранении
- Повышение стойкости яиц при хранении
- Продукты переработки яиц
- Изменения яйца при хранении
- Химический состав яйца
- Химия яйца
- Сальные железы
- Потовые железы
- Использование креатина
- Химия кожного покрова и его производных
- Гормоны задней доли гипофиза
- Гормональные препараты передней доли гипофиза
- Гипофиз (мозговой придаток)
- Половые железы
- Надпочечные железы
- Поджелудочная железа
- Паращитовидные железы
- Щитовидная железа
- Железы внутренней секреции